图3
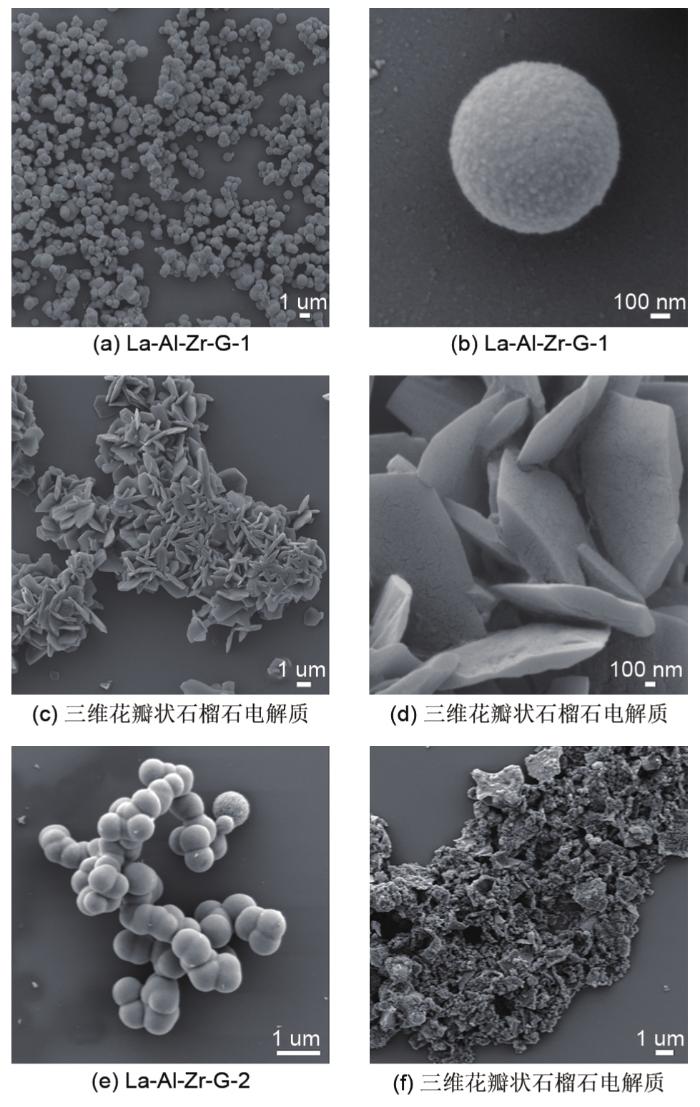
La-Al-Zr-G-x (x =12 )(a, b, e )和三维花瓣状石榴石电解质(c, d, f )的SEM 图及放大图
Fig. 3
The SEM image of La-Al-Zr-G-x (a, b, e ) and three-dimensional petaloid garnet electrolytes (c, d, f)
[1]
ZHANG X, WANG S, XUE C, et al. Self-suppression of lithium dendrite in all-solid-state lithium metal batteries with poly(vinylidene difluoride)-based solid electrolytes[J]. Advanced Materials, 2019, 31(11): doi: 10.1002/adma.201806082.
[本文引用: 1]
[2]
QUARTARONE E, MUSTARELLI P. Electrolytes for solid-state lithium rechargeable batteries: Recent advances and perspectives[J]. Chemical Society Reviews, 2011, 40(5): 2525-2540.
[本文引用: 2]
[3]
ZHANG Q Q, LIU K, DING F, et al. Recent advances in solid polymer electrolytes for lithium batteries[J]. Nano Research, 2017, 10(12): 4139-4174.
[本文引用: 1]
[4]
WANG H, SHENG L, YASIN G, et al. Reviewing the current status and development of polymer electrolytes for solid-state lithium batteries[J]. Energy Storage Materials, 2020, 33: 188-215.
[本文引用: 1]
[5]
MURUGAN R, THANGADURAI V, WEPPNER W. Fast lithium ion conduction in garnet-type Li7 La3 Zr2 O12 [J]. Angewandte Chemie-International Edition, 2007, 46(41): 7778-7781.
[本文引用: 1]
[6]
THANGADURAI V, NARAYANAN S, PINZARU D. Garnet-type solid-state fast Li ion conductors for Li batteries: Critical review[J]. Chemical Society Reviews, 2014, 43(13): 4714-4727.
[本文引用: 1]
[7]
RAMAKUMAR S, DEVIANNAPOORANI C, DHIVYA L, et al. Lithium garnets: Synthesis, structure, Li+ conductivity, Li+ dynamics and applications[J]. Progress in Materials Science, 2017, 88: 325-411.
[本文引用: 1]
[8]
AWAKA J, KIJIMA N, HAYAKAWA H, et al. Synthesis and structure analysis of tetragonal Li7 La3 Zr2 O12 with the garnet-related type structure[J]. Journal of Solid State Chemistry, 2009, 182(8): 2046-2052.
[本文引用: 1]
[9]
WOLFENSTINE J, RANGASAMY E, ALLEN J L, et al. High conductivity of dense tetragonal Li7 La3 Zr2 O12 [J]. Journal of Power Sources, 2012, 208: 193-196.
[本文引用: 1]
[10]
RANGASAMY E, WOLFENSTINE J, SAKAMOTO J. The role of Al and Li concentration on the formation of cubic garnet solid electrolyte of nominal composition Li7 La3 Zr2 O12 [J]. Solid State Ionics, 2012, 206: 28-32.
[本文引用: 1]
[11]
LI Y, HAN J T, WANG C A, et al. Optimizing Li+ conductivity in a garnet framework[J]. Journal of Materials Chemistry, 2012, 22(30): 15357-15361.
[本文引用: 1]
[12]
SONG S, SHEPTYAKOV D, KORSUNSKY A M, et al. High Li ion conductivity in a garnet-type solid electrolyte via unusual site occupation of the doping Ca ions[J]. Materials & Design, 2016, 93: 232-237.
[本文引用: 1]
[13]
DENG F, WU Y, TANG W, et al. Conformal, nanoscale gamma-Al2 O3 coating of garnet conductors for solid-state lithium batteries[J]. Solid State Ionics, 2019, 342: doi: 10.1016/j.ssi.2019.115063.
[14]
SONG S, WU Y, DONG Z, et al. Multi-substituted garnet-type electrolytes for solid-state lithium batteries[J]. Ceramics International, 2020, 46(4): 5489-5494.
[本文引用: 1]
[15]
ZHENG J, DANG H, FENG X, et al. Li-ion transport in a representative ceramic-polymer-plasticizer composite electrolyte: Li7 La3 Zr2 O12 -polyethylene oxide-tetraethylene glycol dimethyl ether[J]. Journal of Materials Chemistry A, 2017, 5(35): 18457-18463.
[本文引用: 1]
[16]
FU K K, GONG Y, DAI J, et al. Flexible, solid-state, ion-conducting membrane with 3D garnet nanofiber networks for lithium batteries[J]. Proceedings of the National Academy of Sciences of the United States of America, 2016, 113(26): 7094-7099.
[本文引用: 1]
[17]
LI Y, ZHANG W, DOU Q Q, et al. Li7 La3 Zr2 O12 ceramic nanofiber-incorporated composite polymer electrolytes for lithium metal batteries[J]. Journal of Materials Chemistry A, 2019, 7(7): 3391-3398.
[本文引用: 1]
[18]
YANG T, ZHENG J, CHENG Q, et al. Composite polymer electrolytes with Li7 La3 Zr2 O12 garnet-type nanowires as ceramic fillers: Mechanism of conductivity enhancement and role of doping and morphology[J]. ACS Applied Materials & Interfaces, 2017, 9(26): 21773-21780.
[本文引用: 1]
[19]
KOTOBUKI M, KOISHI M. Preparation of Li1.5 Al0.5 Ge1.5 (PO4 )3 solid electrolytes via the co-precipitation method[J]. Journal of Asian Ceramic Societies, 2019, 7(4): 551-557.
[本文引用: 1]
[20]
ZHAI H, XU P, NING M, et al. A flexible solid composite electrolyte with vertically aligned and connected ion-conducting nanoparticles for lithium batteries[J]. Nano Letters, 2017, 17(5): 3182-3187.
[本文引用: 1]
[21]
LIU K, WU M, JIANG H, et al. An ultrathin, strong, flexible composite solid electrolyte for high-voltage lithium metal batteries[J]. Journal of Materials Chemistry A, 2020, 8(36): 18802-18809.
[本文引用: 1]
[22]
ZHANG X, LIU T, ZHANG S, et al. Synergistic coupling between Li6.75 La3 Zr1.75 Ta0.25 O12 and poly(vinylidene fluoride) induces high ionic conductivity, mechanical strength, and thermal stability of solid composite electrolytes[J]. Journal of the American Chemical Society, 2017, 139(39): 13779-13785.
[本文引用: 1]
[23]
XU D, SU J, JIN J, et al. In situ generated fireproof gel polymer electrolyte with Li6.4 Ga0.2 La3 Zr2 O12 as initiator and ion-conductive filler[J]. Advanced Energy Materials, 2019, 9 (25): doi: 10.1002/aenm.201900611.
[本文引用: 1]
[24]
YANG X, SUN Q, ZHAO C, et al. High-areal-capacity all-solid-state lithium batteries enabled by rational design of fast ion transport channels in vertically-aligned composite polymer electrodes[J]. Nano Energy, 2019, 61: 567-575.
[本文引用: 1]
[25]
WAN Z, LEI D, YANG W, et al. Low resistance-integrated all-solid-state battery achieved by Li7 La3 Zr2 O12 nanowire upgrading polyethylene oxide (PEO) composite electrolyte and PEO cathode binder[J]. Advanced Functional Materials, 2019, 29(1): doi: 10.1002/adfm.201805301.
[本文引用: 1]
[26]
CHEN L, LI Y, LI S P, et al. PEO/garnet composite electrolytes for solid-state lithium batteries: From "ceramic-in-polymer" to "polymer-in-ceramic"[J]. Nano Energy, 2018, 46: 176-184.
[本文引用: 1]
[27]
LI W W, SUN C Z, JIN J, et al. Realization of the Li+ domain diffusion effect via constructing molecular brushes on the LLZTO surface and its application in all-solid-state lithium batteries[J]. Journal of Materials Chemistry A, 2019, 7(48): 27304-27312.
[本文引用: 1]
[28]
ZHU L, ZHU P, FANG Q, et al. A novel solid PEO/LLTO-nanowires polymer composite electrolyte for solid-state lithium-ion battery[J]. Electrochimica Acta, 2018, 292: 718-726.
[本文引用: 1]
[29]
SONG S, WU Y, TANG W, et al. Composite solid polymer electrolyte with garnet nanosheets in poly(ethylene oxide)[J]. ACS Sustainable Chemistry & Engineering, 2019, 7(7): 7163-7170.
[本文引用: 1]
[30]
WANG X, ZHANG Y, ZHANG X, et al. Lithium-salt-rich PEO/Li0.3 La0.557 TiO3 interpenetrating composite electrolyte with three-dimensional ceramic nano-backbone for all-solid-state lithium-ion batteries[J]. ACS Applied Materials & Interfaces, 2018, 10(29): 24791-24798.
[本文引用: 1]
[31]
SAPTIAMA I, KANETI Y V, SUZUKI Y, et al. Template-free fabrication of mesoporous alumina nanospheres using post-synthesis water-ethanol treatment of monodispersed aluminium glycerate nanospheres for molybdenum adsorption[J]. Small, 2018, 14(21): doi: 10.1002/smll.201800474.
[本文引用: 2]
[32]
MA F X, HU H, WU H B, et al. Formation of uniform Fe3 O4 hollow spheres organized by ultrathin nanosheets and their excellent lithium storage properties[J]. Advanced Materials, 2015, 27(27): 4097-4101.
[本文引用: 1]
[33]
SEPTIANI N L W, KANETI Y V, FATHONI K B, et al. Self-assembly of nickel phosphate-based nanotubes into two-dimensional crumpled sheet-like architectures for high-performance asymmetric supercapacitors[J]. Nano Energy, 2020, 67: doi: 10.1016/j.nanoen.2019.104270.
[本文引用: 1]
[34]
SHEN L, YU L, WU H B, et al. Formation of nickel cobalt sulfide ball-in-ball hollow spheres with enhanced electrochemical pseudocapacitive properties[J]. Nature Communications, 2015, 6: doi: 10.1038/ncomms7694.
[本文引用: 1]
[35]
LI Z, HUANG H M, ZHU J K, et al. Ionic conduction in composite polymer electrolytes: Case of PEO: Ga-LLZO composites[J]. ACS Applied Materials & Interfaces, 2019, 11(1): 784-791.
[本文引用: 1]
1
... 可充电锂离子电池在便携式电子产品、电动汽车以及大型能量存储系统中是重要的存储装置,随着经济社会的快速发展,高能量密度、高安全性以及低成本成为下一代锂离子电池发展的追求目标[1 -2 ] .金属锂的理论比容量高达3860 mA· h/g,密度仅为0.53 g/cm3 ,对标准氢电极电位低至-3.04 V,而且负极可以作为锂源,最大化地利用锂活性物质,避免了石墨类负极材料只是作为锂的脱嵌骨架的问题,所有这些属性使得金属锂成为锂离子电池理想的负极材料.目前应用的锂离子电池使用的是有机液态电解质,虽然具有宽电化学稳定窗口以及较高的能量密度和功率密度,但是有机液态电解质容易与金属锂发生反应,导致金属锂的不稳定沉积以及锂枝晶的生长,最终刺破隔膜使电池短路,出现热失控现象[3 ] .且液态电解质在运输以及使用的过程中容易泄漏、易燃.与液态电解质相比,固态电解质不易燃、无腐蚀、不挥发,拥有良好的绝缘性能,在高温下不发生副反应,因此安全性有了质的提高.再者,由于固态电解质强度较高,在一定程度上可以抑制锂枝晶的生长,从而大幅度提升电池的循环性能[4 ] .因此,固态电解质的成功开发为高安全性、高能量密度、低成本的可充电电池的应用提供了可能. ...
2
... 可充电锂离子电池在便携式电子产品、电动汽车以及大型能量存储系统中是重要的存储装置,随着经济社会的快速发展,高能量密度、高安全性以及低成本成为下一代锂离子电池发展的追求目标[1 -2 ] .金属锂的理论比容量高达3860 mA· h/g,密度仅为0.53 g/cm3 ,对标准氢电极电位低至-3.04 V,而且负极可以作为锂源,最大化地利用锂活性物质,避免了石墨类负极材料只是作为锂的脱嵌骨架的问题,所有这些属性使得金属锂成为锂离子电池理想的负极材料.目前应用的锂离子电池使用的是有机液态电解质,虽然具有宽电化学稳定窗口以及较高的能量密度和功率密度,但是有机液态电解质容易与金属锂发生反应,导致金属锂的不稳定沉积以及锂枝晶的生长,最终刺破隔膜使电池短路,出现热失控现象[3 ] .且液态电解质在运输以及使用的过程中容易泄漏、易燃.与液态电解质相比,固态电解质不易燃、无腐蚀、不挥发,拥有良好的绝缘性能,在高温下不发生副反应,因此安全性有了质的提高.再者,由于固态电解质强度较高,在一定程度上可以抑制锂枝晶的生长,从而大幅度提升电池的循环性能[4 ] .因此,固态电解质的成功开发为高安全性、高能量密度、低成本的可充电电池的应用提供了可能. ...
... 将无机固态电解质与聚合物电解质合理地组合在一起,可以有效地将两种电解质的优点整合在一起,同时避免两者的缺点,制备复合电解质,是目前的解决方法之一.温兆银团队[23 ] 以石榴石型电解质粉体作为引发剂,PVDF‐HFP原位交联聚合,获得了高性能的防火凝胶电解质,以金属锂作为负极、NCM523为正极,结合该电解质,0.5 C倍率循环360周,容量保持率仍高达94.08%.在产业界,星盈科技选择了氧化物-聚合物复合固态电解质的研究路径,通过高温烧结合成LLZTO粉体,采用溶液浇铸法制备出厚度20~100 um的有机-无机复合电解质.基于此,开发了PVDF基-高镍NCM/Li固态电池体系,该体系采用NCM811原位液相包覆和金属锂负极保护层涂覆的开发策略,该电池0.1 C首次放电容量达190 mA· h/g,0.5 C循环寿命可达200周.PEO基聚合物电解质由于其柔韧性、制备简单以及成本低等优点,是近来聚合物电解质的研究热点.然而PEO基电解质在室温下电导率较低,升高温度后虽然可以提高电导率,但是由于其力学性能随之变差,不能有效地阻止锂枝晶生长,为了克服这些缺点,加入无机固态电解质是一种行之有效的策略[2 , 24 -25 ] .众多的填料从维度上可以分为0D的纳米颗粒,1D纳米线,2D纳米片以及3D纳米网络.Fan等[26 ] 采用热压法制备了石榴石纳米颗粒不同含量的PEO基复合电解质,该系列电解质在55 ℃下,以0.2 C的倍率,可以实现高循环效率以及高的容量保持率.温兆银等[27 ] 将石榴石型电解质粉体纳米颗粒与分子刷PMImCl共同与PEO聚合物复合,协同调控电解质填料与聚合物的界面离子传输,显著提升了复合聚合物电解质的电化学性能.Shen等[28 ] 利用静电纺丝制备了1D的石榴石纳米线,且制备了PEO基聚合物,在石榴石纳米线含量为5%时,室温电导率为5.53×10-5 S/cm,电化学窗口为4.75 V,在60 ℃下全电池循环以0.5 C倍率循环100圈后容量保持在123 mA· h/g.胡宁等[29 ] 以石墨烯为模板,利用液相法合成了石榴石纳米片并制备了PEO基聚合物,LLZO纳米片含量为15%且加入离子液体时,室温电导率为3.6×10-4 S/cm,且40 ℃下,全电池循环30圈后容量保持率为97.5%.南策文等[30 ] 利用静电纺丝制备了3D网络结构石榴石,以其为填料制备的PEO基聚合物电解质,室温电导率为1.8×10-4 S/cm,电化学窗口为4.5 V,利用该电解质组装的对称电池,电流密度为0.1 mA/cm2 ,室温下可以有效循环800 h.综上所述,纳米颗粒状、纳米纤维状石榴石型电解质被用来与PEO等聚合物电解质进行复合,从而降低PEO的结晶度,提高电解质的离子电导率,提升PEO基电解质的电化学性能.但是,具有特殊微观形态的石榴石型电解质与PEO的复合研究仍鲜有报道. ...
1
... 可充电锂离子电池在便携式电子产品、电动汽车以及大型能量存储系统中是重要的存储装置,随着经济社会的快速发展,高能量密度、高安全性以及低成本成为下一代锂离子电池发展的追求目标[1 -2 ] .金属锂的理论比容量高达3860 mA· h/g,密度仅为0.53 g/cm3 ,对标准氢电极电位低至-3.04 V,而且负极可以作为锂源,最大化地利用锂活性物质,避免了石墨类负极材料只是作为锂的脱嵌骨架的问题,所有这些属性使得金属锂成为锂离子电池理想的负极材料.目前应用的锂离子电池使用的是有机液态电解质,虽然具有宽电化学稳定窗口以及较高的能量密度和功率密度,但是有机液态电解质容易与金属锂发生反应,导致金属锂的不稳定沉积以及锂枝晶的生长,最终刺破隔膜使电池短路,出现热失控现象[3 ] .且液态电解质在运输以及使用的过程中容易泄漏、易燃.与液态电解质相比,固态电解质不易燃、无腐蚀、不挥发,拥有良好的绝缘性能,在高温下不发生副反应,因此安全性有了质的提高.再者,由于固态电解质强度较高,在一定程度上可以抑制锂枝晶的生长,从而大幅度提升电池的循环性能[4 ] .因此,固态电解质的成功开发为高安全性、高能量密度、低成本的可充电电池的应用提供了可能. ...
1
... 可充电锂离子电池在便携式电子产品、电动汽车以及大型能量存储系统中是重要的存储装置,随着经济社会的快速发展,高能量密度、高安全性以及低成本成为下一代锂离子电池发展的追求目标[1 -2 ] .金属锂的理论比容量高达3860 mA· h/g,密度仅为0.53 g/cm3 ,对标准氢电极电位低至-3.04 V,而且负极可以作为锂源,最大化地利用锂活性物质,避免了石墨类负极材料只是作为锂的脱嵌骨架的问题,所有这些属性使得金属锂成为锂离子电池理想的负极材料.目前应用的锂离子电池使用的是有机液态电解质,虽然具有宽电化学稳定窗口以及较高的能量密度和功率密度,但是有机液态电解质容易与金属锂发生反应,导致金属锂的不稳定沉积以及锂枝晶的生长,最终刺破隔膜使电池短路,出现热失控现象[3 ] .且液态电解质在运输以及使用的过程中容易泄漏、易燃.与液态电解质相比,固态电解质不易燃、无腐蚀、不挥发,拥有良好的绝缘性能,在高温下不发生副反应,因此安全性有了质的提高.再者,由于固态电解质强度较高,在一定程度上可以抑制锂枝晶的生长,从而大幅度提升电池的循环性能[4 ] .因此,固态电解质的成功开发为高安全性、高能量密度、低成本的可充电电池的应用提供了可能. ...
1
... 氧化物型电解质最具前景的为石榴石型、LISICON型、NASICON型三种.石榴石型电解质 Li7 La3 Zr2 O12 是一类具有优异性能的无机陶瓷电解质,被Weppner等[5 ] 于2007年报道.国内外对石榴石型电解质立方相稳定、烧结致密化、晶体结构、离子传输机理的研究比较多[6 -7 ] .石榴石型电解质存在高温介稳立方相和低温/室温稳定四方相[8 ] ,四方相锂位置被100%占据,立方相存在锂空位,造成四方相石榴石离子电导率比立方相低2个数量级[9 ] .稳定立方相石榴石的一个手段是直接掺杂取代Li,产生锂空位.研究表明,0.2~0.24 mol的Al产生0.4~0.48的锂空位可以有效稳定立方相石榴石[10 ] .另一个手段是采用高价离子取代Zr4+ .Li等[11 ] 利用固相法制备Ta掺杂Li7- x 3 Zr2- x x 12 ,发现0.4≤x ≤0.6组成范围内,可实现立方相稳定,具有接近10-3 S/cm的高离子电导率.本文作者团队[12 -14 ] 研究了元素掺杂、碱土氧化物-ZrO2 固溶、放电等离子烧结、Al2 O3 包覆,石榴石离子电导率达1.18×10-3 S/cm.除了固相反应法,研究人员也采用液相法合成纳米颗粒石榴石,电纺丝法合成纤维状石榴石型电解质,如Hu等[15 ] 采用溶胶-凝胶法获得石榴石型电解质,与PEO-TEGDME制备成复合电解质,Hu等[16 ] 首次采用电纺丝法制备了纤维状石榴石型电解质,石榴石纤维经过高温煅烧后,交织在一起,形成三维网络体,PEO-LiTFSI聚合物填充在孔隙中,形成复合固体电解质,离子电导率提高至2.5×10-4 S/cm,这样形成的三维网络体虽然可以提高复合电解质的离子电导率,但是在一定程度上复合电解质存在陶瓷的脆性问题.利用电纺丝法,也同样可以获得石榴石纤维的粉体形态,与PVDF 制备成凝胶电解质[17 ] ,或者与PAN制备成固体电解质[18 ] ,电化学性能都得到改善.可以发现,石榴石型电解质合成方法的研究较少,特别是具有特征微观形态的石榴石型电解质的研究较少. ...
1
... 氧化物型电解质最具前景的为石榴石型、LISICON型、NASICON型三种.石榴石型电解质 Li7 La3 Zr2 O12 是一类具有优异性能的无机陶瓷电解质,被Weppner等[5 ] 于2007年报道.国内外对石榴石型电解质立方相稳定、烧结致密化、晶体结构、离子传输机理的研究比较多[6 -7 ] .石榴石型电解质存在高温介稳立方相和低温/室温稳定四方相[8 ] ,四方相锂位置被100%占据,立方相存在锂空位,造成四方相石榴石离子电导率比立方相低2个数量级[9 ] .稳定立方相石榴石的一个手段是直接掺杂取代Li,产生锂空位.研究表明,0.2~0.24 mol的Al产生0.4~0.48的锂空位可以有效稳定立方相石榴石[10 ] .另一个手段是采用高价离子取代Zr4+ .Li等[11 ] 利用固相法制备Ta掺杂Li7- x 3 Zr2- x x 12 ,发现0.4≤x ≤0.6组成范围内,可实现立方相稳定,具有接近10-3 S/cm的高离子电导率.本文作者团队[12 -14 ] 研究了元素掺杂、碱土氧化物-ZrO2 固溶、放电等离子烧结、Al2 O3 包覆,石榴石离子电导率达1.18×10-3 S/cm.除了固相反应法,研究人员也采用液相法合成纳米颗粒石榴石,电纺丝法合成纤维状石榴石型电解质,如Hu等[15 ] 采用溶胶-凝胶法获得石榴石型电解质,与PEO-TEGDME制备成复合电解质,Hu等[16 ] 首次采用电纺丝法制备了纤维状石榴石型电解质,石榴石纤维经过高温煅烧后,交织在一起,形成三维网络体,PEO-LiTFSI聚合物填充在孔隙中,形成复合固体电解质,离子电导率提高至2.5×10-4 S/cm,这样形成的三维网络体虽然可以提高复合电解质的离子电导率,但是在一定程度上复合电解质存在陶瓷的脆性问题.利用电纺丝法,也同样可以获得石榴石纤维的粉体形态,与PVDF 制备成凝胶电解质[17 ] ,或者与PAN制备成固体电解质[18 ] ,电化学性能都得到改善.可以发现,石榴石型电解质合成方法的研究较少,特别是具有特征微观形态的石榴石型电解质的研究较少. ...
1
... 氧化物型电解质最具前景的为石榴石型、LISICON型、NASICON型三种.石榴石型电解质 Li7 La3 Zr2 O12 是一类具有优异性能的无机陶瓷电解质,被Weppner等[5 ] 于2007年报道.国内外对石榴石型电解质立方相稳定、烧结致密化、晶体结构、离子传输机理的研究比较多[6 -7 ] .石榴石型电解质存在高温介稳立方相和低温/室温稳定四方相[8 ] ,四方相锂位置被100%占据,立方相存在锂空位,造成四方相石榴石离子电导率比立方相低2个数量级[9 ] .稳定立方相石榴石的一个手段是直接掺杂取代Li,产生锂空位.研究表明,0.2~0.24 mol的Al产生0.4~0.48的锂空位可以有效稳定立方相石榴石[10 ] .另一个手段是采用高价离子取代Zr4+ .Li等[11 ] 利用固相法制备Ta掺杂Li7- x 3 Zr2- x x 12 ,发现0.4≤x ≤0.6组成范围内,可实现立方相稳定,具有接近10-3 S/cm的高离子电导率.本文作者团队[12 -14 ] 研究了元素掺杂、碱土氧化物-ZrO2 固溶、放电等离子烧结、Al2 O3 包覆,石榴石离子电导率达1.18×10-3 S/cm.除了固相反应法,研究人员也采用液相法合成纳米颗粒石榴石,电纺丝法合成纤维状石榴石型电解质,如Hu等[15 ] 采用溶胶-凝胶法获得石榴石型电解质,与PEO-TEGDME制备成复合电解质,Hu等[16 ] 首次采用电纺丝法制备了纤维状石榴石型电解质,石榴石纤维经过高温煅烧后,交织在一起,形成三维网络体,PEO-LiTFSI聚合物填充在孔隙中,形成复合固体电解质,离子电导率提高至2.5×10-4 S/cm,这样形成的三维网络体虽然可以提高复合电解质的离子电导率,但是在一定程度上复合电解质存在陶瓷的脆性问题.利用电纺丝法,也同样可以获得石榴石纤维的粉体形态,与PVDF 制备成凝胶电解质[17 ] ,或者与PAN制备成固体电解质[18 ] ,电化学性能都得到改善.可以发现,石榴石型电解质合成方法的研究较少,特别是具有特征微观形态的石榴石型电解质的研究较少. ...
1
... 氧化物型电解质最具前景的为石榴石型、LISICON型、NASICON型三种.石榴石型电解质 Li7 La3 Zr2 O12 是一类具有优异性能的无机陶瓷电解质,被Weppner等[5 ] 于2007年报道.国内外对石榴石型电解质立方相稳定、烧结致密化、晶体结构、离子传输机理的研究比较多[6 -7 ] .石榴石型电解质存在高温介稳立方相和低温/室温稳定四方相[8 ] ,四方相锂位置被100%占据,立方相存在锂空位,造成四方相石榴石离子电导率比立方相低2个数量级[9 ] .稳定立方相石榴石的一个手段是直接掺杂取代Li,产生锂空位.研究表明,0.2~0.24 mol的Al产生0.4~0.48的锂空位可以有效稳定立方相石榴石[10 ] .另一个手段是采用高价离子取代Zr4+ .Li等[11 ] 利用固相法制备Ta掺杂Li7- x 3 Zr2- x x 12 ,发现0.4≤x ≤0.6组成范围内,可实现立方相稳定,具有接近10-3 S/cm的高离子电导率.本文作者团队[12 -14 ] 研究了元素掺杂、碱土氧化物-ZrO2 固溶、放电等离子烧结、Al2 O3 包覆,石榴石离子电导率达1.18×10-3 S/cm.除了固相反应法,研究人员也采用液相法合成纳米颗粒石榴石,电纺丝法合成纤维状石榴石型电解质,如Hu等[15 ] 采用溶胶-凝胶法获得石榴石型电解质,与PEO-TEGDME制备成复合电解质,Hu等[16 ] 首次采用电纺丝法制备了纤维状石榴石型电解质,石榴石纤维经过高温煅烧后,交织在一起,形成三维网络体,PEO-LiTFSI聚合物填充在孔隙中,形成复合固体电解质,离子电导率提高至2.5×10-4 S/cm,这样形成的三维网络体虽然可以提高复合电解质的离子电导率,但是在一定程度上复合电解质存在陶瓷的脆性问题.利用电纺丝法,也同样可以获得石榴石纤维的粉体形态,与PVDF 制备成凝胶电解质[17 ] ,或者与PAN制备成固体电解质[18 ] ,电化学性能都得到改善.可以发现,石榴石型电解质合成方法的研究较少,特别是具有特征微观形态的石榴石型电解质的研究较少. ...
1
... 氧化物型电解质最具前景的为石榴石型、LISICON型、NASICON型三种.石榴石型电解质 Li7 La3 Zr2 O12 是一类具有优异性能的无机陶瓷电解质,被Weppner等[5 ] 于2007年报道.国内外对石榴石型电解质立方相稳定、烧结致密化、晶体结构、离子传输机理的研究比较多[6 -7 ] .石榴石型电解质存在高温介稳立方相和低温/室温稳定四方相[8 ] ,四方相锂位置被100%占据,立方相存在锂空位,造成四方相石榴石离子电导率比立方相低2个数量级[9 ] .稳定立方相石榴石的一个手段是直接掺杂取代Li,产生锂空位.研究表明,0.2~0.24 mol的Al产生0.4~0.48的锂空位可以有效稳定立方相石榴石[10 ] .另一个手段是采用高价离子取代Zr4+ .Li等[11 ] 利用固相法制备Ta掺杂Li7- x 3 Zr2- x x 12 ,发现0.4≤x ≤0.6组成范围内,可实现立方相稳定,具有接近10-3 S/cm的高离子电导率.本文作者团队[12 -14 ] 研究了元素掺杂、碱土氧化物-ZrO2 固溶、放电等离子烧结、Al2 O3 包覆,石榴石离子电导率达1.18×10-3 S/cm.除了固相反应法,研究人员也采用液相法合成纳米颗粒石榴石,电纺丝法合成纤维状石榴石型电解质,如Hu等[15 ] 采用溶胶-凝胶法获得石榴石型电解质,与PEO-TEGDME制备成复合电解质,Hu等[16 ] 首次采用电纺丝法制备了纤维状石榴石型电解质,石榴石纤维经过高温煅烧后,交织在一起,形成三维网络体,PEO-LiTFSI聚合物填充在孔隙中,形成复合固体电解质,离子电导率提高至2.5×10-4 S/cm,这样形成的三维网络体虽然可以提高复合电解质的离子电导率,但是在一定程度上复合电解质存在陶瓷的脆性问题.利用电纺丝法,也同样可以获得石榴石纤维的粉体形态,与PVDF 制备成凝胶电解质[17 ] ,或者与PAN制备成固体电解质[18 ] ,电化学性能都得到改善.可以发现,石榴石型电解质合成方法的研究较少,特别是具有特征微观形态的石榴石型电解质的研究较少. ...
1
... 氧化物型电解质最具前景的为石榴石型、LISICON型、NASICON型三种.石榴石型电解质 Li7 La3 Zr2 O12 是一类具有优异性能的无机陶瓷电解质,被Weppner等[5 ] 于2007年报道.国内外对石榴石型电解质立方相稳定、烧结致密化、晶体结构、离子传输机理的研究比较多[6 -7 ] .石榴石型电解质存在高温介稳立方相和低温/室温稳定四方相[8 ] ,四方相锂位置被100%占据,立方相存在锂空位,造成四方相石榴石离子电导率比立方相低2个数量级[9 ] .稳定立方相石榴石的一个手段是直接掺杂取代Li,产生锂空位.研究表明,0.2~0.24 mol的Al产生0.4~0.48的锂空位可以有效稳定立方相石榴石[10 ] .另一个手段是采用高价离子取代Zr4+ .Li等[11 ] 利用固相法制备Ta掺杂Li7- x 3 Zr2- x x 12 ,发现0.4≤x ≤0.6组成范围内,可实现立方相稳定,具有接近10-3 S/cm的高离子电导率.本文作者团队[12 -14 ] 研究了元素掺杂、碱土氧化物-ZrO2 固溶、放电等离子烧结、Al2 O3 包覆,石榴石离子电导率达1.18×10-3 S/cm.除了固相反应法,研究人员也采用液相法合成纳米颗粒石榴石,电纺丝法合成纤维状石榴石型电解质,如Hu等[15 ] 采用溶胶-凝胶法获得石榴石型电解质,与PEO-TEGDME制备成复合电解质,Hu等[16 ] 首次采用电纺丝法制备了纤维状石榴石型电解质,石榴石纤维经过高温煅烧后,交织在一起,形成三维网络体,PEO-LiTFSI聚合物填充在孔隙中,形成复合固体电解质,离子电导率提高至2.5×10-4 S/cm,这样形成的三维网络体虽然可以提高复合电解质的离子电导率,但是在一定程度上复合电解质存在陶瓷的脆性问题.利用电纺丝法,也同样可以获得石榴石纤维的粉体形态,与PVDF 制备成凝胶电解质[17 ] ,或者与PAN制备成固体电解质[18 ] ,电化学性能都得到改善.可以发现,石榴石型电解质合成方法的研究较少,特别是具有特征微观形态的石榴石型电解质的研究较少. ...
1
... 氧化物型电解质最具前景的为石榴石型、LISICON型、NASICON型三种.石榴石型电解质 Li7 La3 Zr2 O12 是一类具有优异性能的无机陶瓷电解质,被Weppner等[5 ] 于2007年报道.国内外对石榴石型电解质立方相稳定、烧结致密化、晶体结构、离子传输机理的研究比较多[6 -7 ] .石榴石型电解质存在高温介稳立方相和低温/室温稳定四方相[8 ] ,四方相锂位置被100%占据,立方相存在锂空位,造成四方相石榴石离子电导率比立方相低2个数量级[9 ] .稳定立方相石榴石的一个手段是直接掺杂取代Li,产生锂空位.研究表明,0.2~0.24 mol的Al产生0.4~0.48的锂空位可以有效稳定立方相石榴石[10 ] .另一个手段是采用高价离子取代Zr4+ .Li等[11 ] 利用固相法制备Ta掺杂Li7- x 3 Zr2- x x 12 ,发现0.4≤x ≤0.6组成范围内,可实现立方相稳定,具有接近10-3 S/cm的高离子电导率.本文作者团队[12 -14 ] 研究了元素掺杂、碱土氧化物-ZrO2 固溶、放电等离子烧结、Al2 O3 包覆,石榴石离子电导率达1.18×10-3 S/cm.除了固相反应法,研究人员也采用液相法合成纳米颗粒石榴石,电纺丝法合成纤维状石榴石型电解质,如Hu等[15 ] 采用溶胶-凝胶法获得石榴石型电解质,与PEO-TEGDME制备成复合电解质,Hu等[16 ] 首次采用电纺丝法制备了纤维状石榴石型电解质,石榴石纤维经过高温煅烧后,交织在一起,形成三维网络体,PEO-LiTFSI聚合物填充在孔隙中,形成复合固体电解质,离子电导率提高至2.5×10-4 S/cm,这样形成的三维网络体虽然可以提高复合电解质的离子电导率,但是在一定程度上复合电解质存在陶瓷的脆性问题.利用电纺丝法,也同样可以获得石榴石纤维的粉体形态,与PVDF 制备成凝胶电解质[17 ] ,或者与PAN制备成固体电解质[18 ] ,电化学性能都得到改善.可以发现,石榴石型电解质合成方法的研究较少,特别是具有特征微观形态的石榴石型电解质的研究较少. ...
1
... 氧化物型电解质最具前景的为石榴石型、LISICON型、NASICON型三种.石榴石型电解质 Li7 La3 Zr2 O12 是一类具有优异性能的无机陶瓷电解质,被Weppner等[5 ] 于2007年报道.国内外对石榴石型电解质立方相稳定、烧结致密化、晶体结构、离子传输机理的研究比较多[6 -7 ] .石榴石型电解质存在高温介稳立方相和低温/室温稳定四方相[8 ] ,四方相锂位置被100%占据,立方相存在锂空位,造成四方相石榴石离子电导率比立方相低2个数量级[9 ] .稳定立方相石榴石的一个手段是直接掺杂取代Li,产生锂空位.研究表明,0.2~0.24 mol的Al产生0.4~0.48的锂空位可以有效稳定立方相石榴石[10 ] .另一个手段是采用高价离子取代Zr4+ .Li等[11 ] 利用固相法制备Ta掺杂Li7- x 3 Zr2- x x 12 ,发现0.4≤x ≤0.6组成范围内,可实现立方相稳定,具有接近10-3 S/cm的高离子电导率.本文作者团队[12 -14 ] 研究了元素掺杂、碱土氧化物-ZrO2 固溶、放电等离子烧结、Al2 O3 包覆,石榴石离子电导率达1.18×10-3 S/cm.除了固相反应法,研究人员也采用液相法合成纳米颗粒石榴石,电纺丝法合成纤维状石榴石型电解质,如Hu等[15 ] 采用溶胶-凝胶法获得石榴石型电解质,与PEO-TEGDME制备成复合电解质,Hu等[16 ] 首次采用电纺丝法制备了纤维状石榴石型电解质,石榴石纤维经过高温煅烧后,交织在一起,形成三维网络体,PEO-LiTFSI聚合物填充在孔隙中,形成复合固体电解质,离子电导率提高至2.5×10-4 S/cm,这样形成的三维网络体虽然可以提高复合电解质的离子电导率,但是在一定程度上复合电解质存在陶瓷的脆性问题.利用电纺丝法,也同样可以获得石榴石纤维的粉体形态,与PVDF 制备成凝胶电解质[17 ] ,或者与PAN制备成固体电解质[18 ] ,电化学性能都得到改善.可以发现,石榴石型电解质合成方法的研究较少,特别是具有特征微观形态的石榴石型电解质的研究较少. ...
1
... 氧化物型电解质最具前景的为石榴石型、LISICON型、NASICON型三种.石榴石型电解质 Li7 La3 Zr2 O12 是一类具有优异性能的无机陶瓷电解质,被Weppner等[5 ] 于2007年报道.国内外对石榴石型电解质立方相稳定、烧结致密化、晶体结构、离子传输机理的研究比较多[6 -7 ] .石榴石型电解质存在高温介稳立方相和低温/室温稳定四方相[8 ] ,四方相锂位置被100%占据,立方相存在锂空位,造成四方相石榴石离子电导率比立方相低2个数量级[9 ] .稳定立方相石榴石的一个手段是直接掺杂取代Li,产生锂空位.研究表明,0.2~0.24 mol的Al产生0.4~0.48的锂空位可以有效稳定立方相石榴石[10 ] .另一个手段是采用高价离子取代Zr4+ .Li等[11 ] 利用固相法制备Ta掺杂Li7- x 3 Zr2- x x 12 ,发现0.4≤x ≤0.6组成范围内,可实现立方相稳定,具有接近10-3 S/cm的高离子电导率.本文作者团队[12 -14 ] 研究了元素掺杂、碱土氧化物-ZrO2 固溶、放电等离子烧结、Al2 O3 包覆,石榴石离子电导率达1.18×10-3 S/cm.除了固相反应法,研究人员也采用液相法合成纳米颗粒石榴石,电纺丝法合成纤维状石榴石型电解质,如Hu等[15 ] 采用溶胶-凝胶法获得石榴石型电解质,与PEO-TEGDME制备成复合电解质,Hu等[16 ] 首次采用电纺丝法制备了纤维状石榴石型电解质,石榴石纤维经过高温煅烧后,交织在一起,形成三维网络体,PEO-LiTFSI聚合物填充在孔隙中,形成复合固体电解质,离子电导率提高至2.5×10-4 S/cm,这样形成的三维网络体虽然可以提高复合电解质的离子电导率,但是在一定程度上复合电解质存在陶瓷的脆性问题.利用电纺丝法,也同样可以获得石榴石纤维的粉体形态,与PVDF 制备成凝胶电解质[17 ] ,或者与PAN制备成固体电解质[18 ] ,电化学性能都得到改善.可以发现,石榴石型电解质合成方法的研究较少,特别是具有特征微观形态的石榴石型电解质的研究较少. ...
1
... 氧化物型电解质最具前景的为石榴石型、LISICON型、NASICON型三种.石榴石型电解质 Li7 La3 Zr2 O12 是一类具有优异性能的无机陶瓷电解质,被Weppner等[5 ] 于2007年报道.国内外对石榴石型电解质立方相稳定、烧结致密化、晶体结构、离子传输机理的研究比较多[6 -7 ] .石榴石型电解质存在高温介稳立方相和低温/室温稳定四方相[8 ] ,四方相锂位置被100%占据,立方相存在锂空位,造成四方相石榴石离子电导率比立方相低2个数量级[9 ] .稳定立方相石榴石的一个手段是直接掺杂取代Li,产生锂空位.研究表明,0.2~0.24 mol的Al产生0.4~0.48的锂空位可以有效稳定立方相石榴石[10 ] .另一个手段是采用高价离子取代Zr4+ .Li等[11 ] 利用固相法制备Ta掺杂Li7- x 3 Zr2- x x 12 ,发现0.4≤x ≤0.6组成范围内,可实现立方相稳定,具有接近10-3 S/cm的高离子电导率.本文作者团队[12 -14 ] 研究了元素掺杂、碱土氧化物-ZrO2 固溶、放电等离子烧结、Al2 O3 包覆,石榴石离子电导率达1.18×10-3 S/cm.除了固相反应法,研究人员也采用液相法合成纳米颗粒石榴石,电纺丝法合成纤维状石榴石型电解质,如Hu等[15 ] 采用溶胶-凝胶法获得石榴石型电解质,与PEO-TEGDME制备成复合电解质,Hu等[16 ] 首次采用电纺丝法制备了纤维状石榴石型电解质,石榴石纤维经过高温煅烧后,交织在一起,形成三维网络体,PEO-LiTFSI聚合物填充在孔隙中,形成复合固体电解质,离子电导率提高至2.5×10-4 S/cm,这样形成的三维网络体虽然可以提高复合电解质的离子电导率,但是在一定程度上复合电解质存在陶瓷的脆性问题.利用电纺丝法,也同样可以获得石榴石纤维的粉体形态,与PVDF 制备成凝胶电解质[17 ] ,或者与PAN制备成固体电解质[18 ] ,电化学性能都得到改善.可以发现,石榴石型电解质合成方法的研究较少,特别是具有特征微观形态的石榴石型电解质的研究较少. ...
1
... 氧化物型电解质最具前景的为石榴石型、LISICON型、NASICON型三种.石榴石型电解质 Li7 La3 Zr2 O12 是一类具有优异性能的无机陶瓷电解质,被Weppner等[5 ] 于2007年报道.国内外对石榴石型电解质立方相稳定、烧结致密化、晶体结构、离子传输机理的研究比较多[6 -7 ] .石榴石型电解质存在高温介稳立方相和低温/室温稳定四方相[8 ] ,四方相锂位置被100%占据,立方相存在锂空位,造成四方相石榴石离子电导率比立方相低2个数量级[9 ] .稳定立方相石榴石的一个手段是直接掺杂取代Li,产生锂空位.研究表明,0.2~0.24 mol的Al产生0.4~0.48的锂空位可以有效稳定立方相石榴石[10 ] .另一个手段是采用高价离子取代Zr4+ .Li等[11 ] 利用固相法制备Ta掺杂Li7- x 3 Zr2- x x 12 ,发现0.4≤x ≤0.6组成范围内,可实现立方相稳定,具有接近10-3 S/cm的高离子电导率.本文作者团队[12 -14 ] 研究了元素掺杂、碱土氧化物-ZrO2 固溶、放电等离子烧结、Al2 O3 包覆,石榴石离子电导率达1.18×10-3 S/cm.除了固相反应法,研究人员也采用液相法合成纳米颗粒石榴石,电纺丝法合成纤维状石榴石型电解质,如Hu等[15 ] 采用溶胶-凝胶法获得石榴石型电解质,与PEO-TEGDME制备成复合电解质,Hu等[16 ] 首次采用电纺丝法制备了纤维状石榴石型电解质,石榴石纤维经过高温煅烧后,交织在一起,形成三维网络体,PEO-LiTFSI聚合物填充在孔隙中,形成复合固体电解质,离子电导率提高至2.5×10-4 S/cm,这样形成的三维网络体虽然可以提高复合电解质的离子电导率,但是在一定程度上复合电解质存在陶瓷的脆性问题.利用电纺丝法,也同样可以获得石榴石纤维的粉体形态,与PVDF 制备成凝胶电解质[17 ] ,或者与PAN制备成固体电解质[18 ] ,电化学性能都得到改善.可以发现,石榴石型电解质合成方法的研究较少,特别是具有特征微观形态的石榴石型电解质的研究较少. ...
1
... 氧化物型电解质最具前景的为石榴石型、LISICON型、NASICON型三种.石榴石型电解质 Li7 La3 Zr2 O12 是一类具有优异性能的无机陶瓷电解质,被Weppner等[5 ] 于2007年报道.国内外对石榴石型电解质立方相稳定、烧结致密化、晶体结构、离子传输机理的研究比较多[6 -7 ] .石榴石型电解质存在高温介稳立方相和低温/室温稳定四方相[8 ] ,四方相锂位置被100%占据,立方相存在锂空位,造成四方相石榴石离子电导率比立方相低2个数量级[9 ] .稳定立方相石榴石的一个手段是直接掺杂取代Li,产生锂空位.研究表明,0.2~0.24 mol的Al产生0.4~0.48的锂空位可以有效稳定立方相石榴石[10 ] .另一个手段是采用高价离子取代Zr4+ .Li等[11 ] 利用固相法制备Ta掺杂Li7- x 3 Zr2- x x 12 ,发现0.4≤x ≤0.6组成范围内,可实现立方相稳定,具有接近10-3 S/cm的高离子电导率.本文作者团队[12 -14 ] 研究了元素掺杂、碱土氧化物-ZrO2 固溶、放电等离子烧结、Al2 O3 包覆,石榴石离子电导率达1.18×10-3 S/cm.除了固相反应法,研究人员也采用液相法合成纳米颗粒石榴石,电纺丝法合成纤维状石榴石型电解质,如Hu等[15 ] 采用溶胶-凝胶法获得石榴石型电解质,与PEO-TEGDME制备成复合电解质,Hu等[16 ] 首次采用电纺丝法制备了纤维状石榴石型电解质,石榴石纤维经过高温煅烧后,交织在一起,形成三维网络体,PEO-LiTFSI聚合物填充在孔隙中,形成复合固体电解质,离子电导率提高至2.5×10-4 S/cm,这样形成的三维网络体虽然可以提高复合电解质的离子电导率,但是在一定程度上复合电解质存在陶瓷的脆性问题.利用电纺丝法,也同样可以获得石榴石纤维的粉体形态,与PVDF 制备成凝胶电解质[17 ] ,或者与PAN制备成固体电解质[18 ] ,电化学性能都得到改善.可以发现,石榴石型电解质合成方法的研究较少,特别是具有特征微观形态的石榴石型电解质的研究较少. ...
1
... 氧化物型电解质最具前景的为石榴石型、LISICON型、NASICON型三种.石榴石型电解质 Li7 La3 Zr2 O12 是一类具有优异性能的无机陶瓷电解质,被Weppner等[5 ] 于2007年报道.国内外对石榴石型电解质立方相稳定、烧结致密化、晶体结构、离子传输机理的研究比较多[6 -7 ] .石榴石型电解质存在高温介稳立方相和低温/室温稳定四方相[8 ] ,四方相锂位置被100%占据,立方相存在锂空位,造成四方相石榴石离子电导率比立方相低2个数量级[9 ] .稳定立方相石榴石的一个手段是直接掺杂取代Li,产生锂空位.研究表明,0.2~0.24 mol的Al产生0.4~0.48的锂空位可以有效稳定立方相石榴石[10 ] .另一个手段是采用高价离子取代Zr4+ .Li等[11 ] 利用固相法制备Ta掺杂Li7- x 3 Zr2- x x 12 ,发现0.4≤x ≤0.6组成范围内,可实现立方相稳定,具有接近10-3 S/cm的高离子电导率.本文作者团队[12 -14 ] 研究了元素掺杂、碱土氧化物-ZrO2 固溶、放电等离子烧结、Al2 O3 包覆,石榴石离子电导率达1.18×10-3 S/cm.除了固相反应法,研究人员也采用液相法合成纳米颗粒石榴石,电纺丝法合成纤维状石榴石型电解质,如Hu等[15 ] 采用溶胶-凝胶法获得石榴石型电解质,与PEO-TEGDME制备成复合电解质,Hu等[16 ] 首次采用电纺丝法制备了纤维状石榴石型电解质,石榴石纤维经过高温煅烧后,交织在一起,形成三维网络体,PEO-LiTFSI聚合物填充在孔隙中,形成复合固体电解质,离子电导率提高至2.5×10-4 S/cm,这样形成的三维网络体虽然可以提高复合电解质的离子电导率,但是在一定程度上复合电解质存在陶瓷的脆性问题.利用电纺丝法,也同样可以获得石榴石纤维的粉体形态,与PVDF 制备成凝胶电解质[17 ] ,或者与PAN制备成固体电解质[18 ] ,电化学性能都得到改善.可以发现,石榴石型电解质合成方法的研究较少,特别是具有特征微观形态的石榴石型电解质的研究较少. ...
1
... 石榴石等无机陶瓷电解质具有较高的离子电导率(10-4 ~10-2 S/cm),但是脆性较大、与电极材料的界面电阻较大、制备过程较为复杂.固态聚合物电解质则是另一类具有应用前景的电解质体系,具有制备过程简单、良好的柔软性、良好的电极界面接触性的优点,但是室温电导率较低[19 ] .固态聚合物电解质一般是由聚合物和锂盐混合制备,常用的聚合物基体包括PEO[20 ] 、聚丙烯腈(PAN)[21 ] 、聚偏氟乙烯(PVDF)[22 ] 等.在过去的研究中,无机固态电解质与聚合物电解质都取得了很大的进展,但是将任何单组分的固态电解质应用于二次锂离子电池仍然是很大的挑战. ...
1
... 石榴石等无机陶瓷电解质具有较高的离子电导率(10-4 ~10-2 S/cm),但是脆性较大、与电极材料的界面电阻较大、制备过程较为复杂.固态聚合物电解质则是另一类具有应用前景的电解质体系,具有制备过程简单、良好的柔软性、良好的电极界面接触性的优点,但是室温电导率较低[19 ] .固态聚合物电解质一般是由聚合物和锂盐混合制备,常用的聚合物基体包括PEO[20 ] 、聚丙烯腈(PAN)[21 ] 、聚偏氟乙烯(PVDF)[22 ] 等.在过去的研究中,无机固态电解质与聚合物电解质都取得了很大的进展,但是将任何单组分的固态电解质应用于二次锂离子电池仍然是很大的挑战. ...
1
... 石榴石等无机陶瓷电解质具有较高的离子电导率(10-4 ~10-2 S/cm),但是脆性较大、与电极材料的界面电阻较大、制备过程较为复杂.固态聚合物电解质则是另一类具有应用前景的电解质体系,具有制备过程简单、良好的柔软性、良好的电极界面接触性的优点,但是室温电导率较低[19 ] .固态聚合物电解质一般是由聚合物和锂盐混合制备,常用的聚合物基体包括PEO[20 ] 、聚丙烯腈(PAN)[21 ] 、聚偏氟乙烯(PVDF)[22 ] 等.在过去的研究中,无机固态电解质与聚合物电解质都取得了很大的进展,但是将任何单组分的固态电解质应用于二次锂离子电池仍然是很大的挑战. ...
1
... 石榴石等无机陶瓷电解质具有较高的离子电导率(10-4 ~10-2 S/cm),但是脆性较大、与电极材料的界面电阻较大、制备过程较为复杂.固态聚合物电解质则是另一类具有应用前景的电解质体系,具有制备过程简单、良好的柔软性、良好的电极界面接触性的优点,但是室温电导率较低[19 ] .固态聚合物电解质一般是由聚合物和锂盐混合制备,常用的聚合物基体包括PEO[20 ] 、聚丙烯腈(PAN)[21 ] 、聚偏氟乙烯(PVDF)[22 ] 等.在过去的研究中,无机固态电解质与聚合物电解质都取得了很大的进展,但是将任何单组分的固态电解质应用于二次锂离子电池仍然是很大的挑战. ...
1
... 将无机固态电解质与聚合物电解质合理地组合在一起,可以有效地将两种电解质的优点整合在一起,同时避免两者的缺点,制备复合电解质,是目前的解决方法之一.温兆银团队[23 ] 以石榴石型电解质粉体作为引发剂,PVDF‐HFP原位交联聚合,获得了高性能的防火凝胶电解质,以金属锂作为负极、NCM523为正极,结合该电解质,0.5 C倍率循环360周,容量保持率仍高达94.08%.在产业界,星盈科技选择了氧化物-聚合物复合固态电解质的研究路径,通过高温烧结合成LLZTO粉体,采用溶液浇铸法制备出厚度20~100 um的有机-无机复合电解质.基于此,开发了PVDF基-高镍NCM/Li固态电池体系,该体系采用NCM811原位液相包覆和金属锂负极保护层涂覆的开发策略,该电池0.1 C首次放电容量达190 mA· h/g,0.5 C循环寿命可达200周.PEO基聚合物电解质由于其柔韧性、制备简单以及成本低等优点,是近来聚合物电解质的研究热点.然而PEO基电解质在室温下电导率较低,升高温度后虽然可以提高电导率,但是由于其力学性能随之变差,不能有效地阻止锂枝晶生长,为了克服这些缺点,加入无机固态电解质是一种行之有效的策略[2 , 24 -25 ] .众多的填料从维度上可以分为0D的纳米颗粒,1D纳米线,2D纳米片以及3D纳米网络.Fan等[26 ] 采用热压法制备了石榴石纳米颗粒不同含量的PEO基复合电解质,该系列电解质在55 ℃下,以0.2 C的倍率,可以实现高循环效率以及高的容量保持率.温兆银等[27 ] 将石榴石型电解质粉体纳米颗粒与分子刷PMImCl共同与PEO聚合物复合,协同调控电解质填料与聚合物的界面离子传输,显著提升了复合聚合物电解质的电化学性能.Shen等[28 ] 利用静电纺丝制备了1D的石榴石纳米线,且制备了PEO基聚合物,在石榴石纳米线含量为5%时,室温电导率为5.53×10-5 S/cm,电化学窗口为4.75 V,在60 ℃下全电池循环以0.5 C倍率循环100圈后容量保持在123 mA· h/g.胡宁等[29 ] 以石墨烯为模板,利用液相法合成了石榴石纳米片并制备了PEO基聚合物,LLZO纳米片含量为15%且加入离子液体时,室温电导率为3.6×10-4 S/cm,且40 ℃下,全电池循环30圈后容量保持率为97.5%.南策文等[30 ] 利用静电纺丝制备了3D网络结构石榴石,以其为填料制备的PEO基聚合物电解质,室温电导率为1.8×10-4 S/cm,电化学窗口为4.5 V,利用该电解质组装的对称电池,电流密度为0.1 mA/cm2 ,室温下可以有效循环800 h.综上所述,纳米颗粒状、纳米纤维状石榴石型电解质被用来与PEO等聚合物电解质进行复合,从而降低PEO的结晶度,提高电解质的离子电导率,提升PEO基电解质的电化学性能.但是,具有特殊微观形态的石榴石型电解质与PEO的复合研究仍鲜有报道. ...
1
... 将无机固态电解质与聚合物电解质合理地组合在一起,可以有效地将两种电解质的优点整合在一起,同时避免两者的缺点,制备复合电解质,是目前的解决方法之一.温兆银团队[23 ] 以石榴石型电解质粉体作为引发剂,PVDF‐HFP原位交联聚合,获得了高性能的防火凝胶电解质,以金属锂作为负极、NCM523为正极,结合该电解质,0.5 C倍率循环360周,容量保持率仍高达94.08%.在产业界,星盈科技选择了氧化物-聚合物复合固态电解质的研究路径,通过高温烧结合成LLZTO粉体,采用溶液浇铸法制备出厚度20~100 um的有机-无机复合电解质.基于此,开发了PVDF基-高镍NCM/Li固态电池体系,该体系采用NCM811原位液相包覆和金属锂负极保护层涂覆的开发策略,该电池0.1 C首次放电容量达190 mA· h/g,0.5 C循环寿命可达200周.PEO基聚合物电解质由于其柔韧性、制备简单以及成本低等优点,是近来聚合物电解质的研究热点.然而PEO基电解质在室温下电导率较低,升高温度后虽然可以提高电导率,但是由于其力学性能随之变差,不能有效地阻止锂枝晶生长,为了克服这些缺点,加入无机固态电解质是一种行之有效的策略[2 , 24 -25 ] .众多的填料从维度上可以分为0D的纳米颗粒,1D纳米线,2D纳米片以及3D纳米网络.Fan等[26 ] 采用热压法制备了石榴石纳米颗粒不同含量的PEO基复合电解质,该系列电解质在55 ℃下,以0.2 C的倍率,可以实现高循环效率以及高的容量保持率.温兆银等[27 ] 将石榴石型电解质粉体纳米颗粒与分子刷PMImCl共同与PEO聚合物复合,协同调控电解质填料与聚合物的界面离子传输,显著提升了复合聚合物电解质的电化学性能.Shen等[28 ] 利用静电纺丝制备了1D的石榴石纳米线,且制备了PEO基聚合物,在石榴石纳米线含量为5%时,室温电导率为5.53×10-5 S/cm,电化学窗口为4.75 V,在60 ℃下全电池循环以0.5 C倍率循环100圈后容量保持在123 mA· h/g.胡宁等[29 ] 以石墨烯为模板,利用液相法合成了石榴石纳米片并制备了PEO基聚合物,LLZO纳米片含量为15%且加入离子液体时,室温电导率为3.6×10-4 S/cm,且40 ℃下,全电池循环30圈后容量保持率为97.5%.南策文等[30 ] 利用静电纺丝制备了3D网络结构石榴石,以其为填料制备的PEO基聚合物电解质,室温电导率为1.8×10-4 S/cm,电化学窗口为4.5 V,利用该电解质组装的对称电池,电流密度为0.1 mA/cm2 ,室温下可以有效循环800 h.综上所述,纳米颗粒状、纳米纤维状石榴石型电解质被用来与PEO等聚合物电解质进行复合,从而降低PEO的结晶度,提高电解质的离子电导率,提升PEO基电解质的电化学性能.但是,具有特殊微观形态的石榴石型电解质与PEO的复合研究仍鲜有报道. ...
1
... 将无机固态电解质与聚合物电解质合理地组合在一起,可以有效地将两种电解质的优点整合在一起,同时避免两者的缺点,制备复合电解质,是目前的解决方法之一.温兆银团队[23 ] 以石榴石型电解质粉体作为引发剂,PVDF‐HFP原位交联聚合,获得了高性能的防火凝胶电解质,以金属锂作为负极、NCM523为正极,结合该电解质,0.5 C倍率循环360周,容量保持率仍高达94.08%.在产业界,星盈科技选择了氧化物-聚合物复合固态电解质的研究路径,通过高温烧结合成LLZTO粉体,采用溶液浇铸法制备出厚度20~100 um的有机-无机复合电解质.基于此,开发了PVDF基-高镍NCM/Li固态电池体系,该体系采用NCM811原位液相包覆和金属锂负极保护层涂覆的开发策略,该电池0.1 C首次放电容量达190 mA· h/g,0.5 C循环寿命可达200周.PEO基聚合物电解质由于其柔韧性、制备简单以及成本低等优点,是近来聚合物电解质的研究热点.然而PEO基电解质在室温下电导率较低,升高温度后虽然可以提高电导率,但是由于其力学性能随之变差,不能有效地阻止锂枝晶生长,为了克服这些缺点,加入无机固态电解质是一种行之有效的策略[2 , 24 -25 ] .众多的填料从维度上可以分为0D的纳米颗粒,1D纳米线,2D纳米片以及3D纳米网络.Fan等[26 ] 采用热压法制备了石榴石纳米颗粒不同含量的PEO基复合电解质,该系列电解质在55 ℃下,以0.2 C的倍率,可以实现高循环效率以及高的容量保持率.温兆银等[27 ] 将石榴石型电解质粉体纳米颗粒与分子刷PMImCl共同与PEO聚合物复合,协同调控电解质填料与聚合物的界面离子传输,显著提升了复合聚合物电解质的电化学性能.Shen等[28 ] 利用静电纺丝制备了1D的石榴石纳米线,且制备了PEO基聚合物,在石榴石纳米线含量为5%时,室温电导率为5.53×10-5 S/cm,电化学窗口为4.75 V,在60 ℃下全电池循环以0.5 C倍率循环100圈后容量保持在123 mA· h/g.胡宁等[29 ] 以石墨烯为模板,利用液相法合成了石榴石纳米片并制备了PEO基聚合物,LLZO纳米片含量为15%且加入离子液体时,室温电导率为3.6×10-4 S/cm,且40 ℃下,全电池循环30圈后容量保持率为97.5%.南策文等[30 ] 利用静电纺丝制备了3D网络结构石榴石,以其为填料制备的PEO基聚合物电解质,室温电导率为1.8×10-4 S/cm,电化学窗口为4.5 V,利用该电解质组装的对称电池,电流密度为0.1 mA/cm2 ,室温下可以有效循环800 h.综上所述,纳米颗粒状、纳米纤维状石榴石型电解质被用来与PEO等聚合物电解质进行复合,从而降低PEO的结晶度,提高电解质的离子电导率,提升PEO基电解质的电化学性能.但是,具有特殊微观形态的石榴石型电解质与PEO的复合研究仍鲜有报道. ...
1
... 将无机固态电解质与聚合物电解质合理地组合在一起,可以有效地将两种电解质的优点整合在一起,同时避免两者的缺点,制备复合电解质,是目前的解决方法之一.温兆银团队[23 ] 以石榴石型电解质粉体作为引发剂,PVDF‐HFP原位交联聚合,获得了高性能的防火凝胶电解质,以金属锂作为负极、NCM523为正极,结合该电解质,0.5 C倍率循环360周,容量保持率仍高达94.08%.在产业界,星盈科技选择了氧化物-聚合物复合固态电解质的研究路径,通过高温烧结合成LLZTO粉体,采用溶液浇铸法制备出厚度20~100 um的有机-无机复合电解质.基于此,开发了PVDF基-高镍NCM/Li固态电池体系,该体系采用NCM811原位液相包覆和金属锂负极保护层涂覆的开发策略,该电池0.1 C首次放电容量达190 mA· h/g,0.5 C循环寿命可达200周.PEO基聚合物电解质由于其柔韧性、制备简单以及成本低等优点,是近来聚合物电解质的研究热点.然而PEO基电解质在室温下电导率较低,升高温度后虽然可以提高电导率,但是由于其力学性能随之变差,不能有效地阻止锂枝晶生长,为了克服这些缺点,加入无机固态电解质是一种行之有效的策略[2 , 24 -25 ] .众多的填料从维度上可以分为0D的纳米颗粒,1D纳米线,2D纳米片以及3D纳米网络.Fan等[26 ] 采用热压法制备了石榴石纳米颗粒不同含量的PEO基复合电解质,该系列电解质在55 ℃下,以0.2 C的倍率,可以实现高循环效率以及高的容量保持率.温兆银等[27 ] 将石榴石型电解质粉体纳米颗粒与分子刷PMImCl共同与PEO聚合物复合,协同调控电解质填料与聚合物的界面离子传输,显著提升了复合聚合物电解质的电化学性能.Shen等[28 ] 利用静电纺丝制备了1D的石榴石纳米线,且制备了PEO基聚合物,在石榴石纳米线含量为5%时,室温电导率为5.53×10-5 S/cm,电化学窗口为4.75 V,在60 ℃下全电池循环以0.5 C倍率循环100圈后容量保持在123 mA· h/g.胡宁等[29 ] 以石墨烯为模板,利用液相法合成了石榴石纳米片并制备了PEO基聚合物,LLZO纳米片含量为15%且加入离子液体时,室温电导率为3.6×10-4 S/cm,且40 ℃下,全电池循环30圈后容量保持率为97.5%.南策文等[30 ] 利用静电纺丝制备了3D网络结构石榴石,以其为填料制备的PEO基聚合物电解质,室温电导率为1.8×10-4 S/cm,电化学窗口为4.5 V,利用该电解质组装的对称电池,电流密度为0.1 mA/cm2 ,室温下可以有效循环800 h.综上所述,纳米颗粒状、纳米纤维状石榴石型电解质被用来与PEO等聚合物电解质进行复合,从而降低PEO的结晶度,提高电解质的离子电导率,提升PEO基电解质的电化学性能.但是,具有特殊微观形态的石榴石型电解质与PEO的复合研究仍鲜有报道. ...
1
... 将无机固态电解质与聚合物电解质合理地组合在一起,可以有效地将两种电解质的优点整合在一起,同时避免两者的缺点,制备复合电解质,是目前的解决方法之一.温兆银团队[23 ] 以石榴石型电解质粉体作为引发剂,PVDF‐HFP原位交联聚合,获得了高性能的防火凝胶电解质,以金属锂作为负极、NCM523为正极,结合该电解质,0.5 C倍率循环360周,容量保持率仍高达94.08%.在产业界,星盈科技选择了氧化物-聚合物复合固态电解质的研究路径,通过高温烧结合成LLZTO粉体,采用溶液浇铸法制备出厚度20~100 um的有机-无机复合电解质.基于此,开发了PVDF基-高镍NCM/Li固态电池体系,该体系采用NCM811原位液相包覆和金属锂负极保护层涂覆的开发策略,该电池0.1 C首次放电容量达190 mA· h/g,0.5 C循环寿命可达200周.PEO基聚合物电解质由于其柔韧性、制备简单以及成本低等优点,是近来聚合物电解质的研究热点.然而PEO基电解质在室温下电导率较低,升高温度后虽然可以提高电导率,但是由于其力学性能随之变差,不能有效地阻止锂枝晶生长,为了克服这些缺点,加入无机固态电解质是一种行之有效的策略[2 , 24 -25 ] .众多的填料从维度上可以分为0D的纳米颗粒,1D纳米线,2D纳米片以及3D纳米网络.Fan等[26 ] 采用热压法制备了石榴石纳米颗粒不同含量的PEO基复合电解质,该系列电解质在55 ℃下,以0.2 C的倍率,可以实现高循环效率以及高的容量保持率.温兆银等[27 ] 将石榴石型电解质粉体纳米颗粒与分子刷PMImCl共同与PEO聚合物复合,协同调控电解质填料与聚合物的界面离子传输,显著提升了复合聚合物电解质的电化学性能.Shen等[28 ] 利用静电纺丝制备了1D的石榴石纳米线,且制备了PEO基聚合物,在石榴石纳米线含量为5%时,室温电导率为5.53×10-5 S/cm,电化学窗口为4.75 V,在60 ℃下全电池循环以0.5 C倍率循环100圈后容量保持在123 mA· h/g.胡宁等[29 ] 以石墨烯为模板,利用液相法合成了石榴石纳米片并制备了PEO基聚合物,LLZO纳米片含量为15%且加入离子液体时,室温电导率为3.6×10-4 S/cm,且40 ℃下,全电池循环30圈后容量保持率为97.5%.南策文等[30 ] 利用静电纺丝制备了3D网络结构石榴石,以其为填料制备的PEO基聚合物电解质,室温电导率为1.8×10-4 S/cm,电化学窗口为4.5 V,利用该电解质组装的对称电池,电流密度为0.1 mA/cm2 ,室温下可以有效循环800 h.综上所述,纳米颗粒状、纳米纤维状石榴石型电解质被用来与PEO等聚合物电解质进行复合,从而降低PEO的结晶度,提高电解质的离子电导率,提升PEO基电解质的电化学性能.但是,具有特殊微观形态的石榴石型电解质与PEO的复合研究仍鲜有报道. ...
1
... 将无机固态电解质与聚合物电解质合理地组合在一起,可以有效地将两种电解质的优点整合在一起,同时避免两者的缺点,制备复合电解质,是目前的解决方法之一.温兆银团队[23 ] 以石榴石型电解质粉体作为引发剂,PVDF‐HFP原位交联聚合,获得了高性能的防火凝胶电解质,以金属锂作为负极、NCM523为正极,结合该电解质,0.5 C倍率循环360周,容量保持率仍高达94.08%.在产业界,星盈科技选择了氧化物-聚合物复合固态电解质的研究路径,通过高温烧结合成LLZTO粉体,采用溶液浇铸法制备出厚度20~100 um的有机-无机复合电解质.基于此,开发了PVDF基-高镍NCM/Li固态电池体系,该体系采用NCM811原位液相包覆和金属锂负极保护层涂覆的开发策略,该电池0.1 C首次放电容量达190 mA· h/g,0.5 C循环寿命可达200周.PEO基聚合物电解质由于其柔韧性、制备简单以及成本低等优点,是近来聚合物电解质的研究热点.然而PEO基电解质在室温下电导率较低,升高温度后虽然可以提高电导率,但是由于其力学性能随之变差,不能有效地阻止锂枝晶生长,为了克服这些缺点,加入无机固态电解质是一种行之有效的策略[2 , 24 -25 ] .众多的填料从维度上可以分为0D的纳米颗粒,1D纳米线,2D纳米片以及3D纳米网络.Fan等[26 ] 采用热压法制备了石榴石纳米颗粒不同含量的PEO基复合电解质,该系列电解质在55 ℃下,以0.2 C的倍率,可以实现高循环效率以及高的容量保持率.温兆银等[27 ] 将石榴石型电解质粉体纳米颗粒与分子刷PMImCl共同与PEO聚合物复合,协同调控电解质填料与聚合物的界面离子传输,显著提升了复合聚合物电解质的电化学性能.Shen等[28 ] 利用静电纺丝制备了1D的石榴石纳米线,且制备了PEO基聚合物,在石榴石纳米线含量为5%时,室温电导率为5.53×10-5 S/cm,电化学窗口为4.75 V,在60 ℃下全电池循环以0.5 C倍率循环100圈后容量保持在123 mA· h/g.胡宁等[29 ] 以石墨烯为模板,利用液相法合成了石榴石纳米片并制备了PEO基聚合物,LLZO纳米片含量为15%且加入离子液体时,室温电导率为3.6×10-4 S/cm,且40 ℃下,全电池循环30圈后容量保持率为97.5%.南策文等[30 ] 利用静电纺丝制备了3D网络结构石榴石,以其为填料制备的PEO基聚合物电解质,室温电导率为1.8×10-4 S/cm,电化学窗口为4.5 V,利用该电解质组装的对称电池,电流密度为0.1 mA/cm2 ,室温下可以有效循环800 h.综上所述,纳米颗粒状、纳米纤维状石榴石型电解质被用来与PEO等聚合物电解质进行复合,从而降低PEO的结晶度,提高电解质的离子电导率,提升PEO基电解质的电化学性能.但是,具有特殊微观形态的石榴石型电解质与PEO的复合研究仍鲜有报道. ...
1
... 将无机固态电解质与聚合物电解质合理地组合在一起,可以有效地将两种电解质的优点整合在一起,同时避免两者的缺点,制备复合电解质,是目前的解决方法之一.温兆银团队[23 ] 以石榴石型电解质粉体作为引发剂,PVDF‐HFP原位交联聚合,获得了高性能的防火凝胶电解质,以金属锂作为负极、NCM523为正极,结合该电解质,0.5 C倍率循环360周,容量保持率仍高达94.08%.在产业界,星盈科技选择了氧化物-聚合物复合固态电解质的研究路径,通过高温烧结合成LLZTO粉体,采用溶液浇铸法制备出厚度20~100 um的有机-无机复合电解质.基于此,开发了PVDF基-高镍NCM/Li固态电池体系,该体系采用NCM811原位液相包覆和金属锂负极保护层涂覆的开发策略,该电池0.1 C首次放电容量达190 mA· h/g,0.5 C循环寿命可达200周.PEO基聚合物电解质由于其柔韧性、制备简单以及成本低等优点,是近来聚合物电解质的研究热点.然而PEO基电解质在室温下电导率较低,升高温度后虽然可以提高电导率,但是由于其力学性能随之变差,不能有效地阻止锂枝晶生长,为了克服这些缺点,加入无机固态电解质是一种行之有效的策略[2 , 24 -25 ] .众多的填料从维度上可以分为0D的纳米颗粒,1D纳米线,2D纳米片以及3D纳米网络.Fan等[26 ] 采用热压法制备了石榴石纳米颗粒不同含量的PEO基复合电解质,该系列电解质在55 ℃下,以0.2 C的倍率,可以实现高循环效率以及高的容量保持率.温兆银等[27 ] 将石榴石型电解质粉体纳米颗粒与分子刷PMImCl共同与PEO聚合物复合,协同调控电解质填料与聚合物的界面离子传输,显著提升了复合聚合物电解质的电化学性能.Shen等[28 ] 利用静电纺丝制备了1D的石榴石纳米线,且制备了PEO基聚合物,在石榴石纳米线含量为5%时,室温电导率为5.53×10-5 S/cm,电化学窗口为4.75 V,在60 ℃下全电池循环以0.5 C倍率循环100圈后容量保持在123 mA· h/g.胡宁等[29 ] 以石墨烯为模板,利用液相法合成了石榴石纳米片并制备了PEO基聚合物,LLZO纳米片含量为15%且加入离子液体时,室温电导率为3.6×10-4 S/cm,且40 ℃下,全电池循环30圈后容量保持率为97.5%.南策文等[30 ] 利用静电纺丝制备了3D网络结构石榴石,以其为填料制备的PEO基聚合物电解质,室温电导率为1.8×10-4 S/cm,电化学窗口为4.5 V,利用该电解质组装的对称电池,电流密度为0.1 mA/cm2 ,室温下可以有效循环800 h.综上所述,纳米颗粒状、纳米纤维状石榴石型电解质被用来与PEO等聚合物电解质进行复合,从而降低PEO的结晶度,提高电解质的离子电导率,提升PEO基电解质的电化学性能.但是,具有特殊微观形态的石榴石型电解质与PEO的复合研究仍鲜有报道. ...
1
... 将无机固态电解质与聚合物电解质合理地组合在一起,可以有效地将两种电解质的优点整合在一起,同时避免两者的缺点,制备复合电解质,是目前的解决方法之一.温兆银团队[23 ] 以石榴石型电解质粉体作为引发剂,PVDF‐HFP原位交联聚合,获得了高性能的防火凝胶电解质,以金属锂作为负极、NCM523为正极,结合该电解质,0.5 C倍率循环360周,容量保持率仍高达94.08%.在产业界,星盈科技选择了氧化物-聚合物复合固态电解质的研究路径,通过高温烧结合成LLZTO粉体,采用溶液浇铸法制备出厚度20~100 um的有机-无机复合电解质.基于此,开发了PVDF基-高镍NCM/Li固态电池体系,该体系采用NCM811原位液相包覆和金属锂负极保护层涂覆的开发策略,该电池0.1 C首次放电容量达190 mA· h/g,0.5 C循环寿命可达200周.PEO基聚合物电解质由于其柔韧性、制备简单以及成本低等优点,是近来聚合物电解质的研究热点.然而PEO基电解质在室温下电导率较低,升高温度后虽然可以提高电导率,但是由于其力学性能随之变差,不能有效地阻止锂枝晶生长,为了克服这些缺点,加入无机固态电解质是一种行之有效的策略[2 , 24 -25 ] .众多的填料从维度上可以分为0D的纳米颗粒,1D纳米线,2D纳米片以及3D纳米网络.Fan等[26 ] 采用热压法制备了石榴石纳米颗粒不同含量的PEO基复合电解质,该系列电解质在55 ℃下,以0.2 C的倍率,可以实现高循环效率以及高的容量保持率.温兆银等[27 ] 将石榴石型电解质粉体纳米颗粒与分子刷PMImCl共同与PEO聚合物复合,协同调控电解质填料与聚合物的界面离子传输,显著提升了复合聚合物电解质的电化学性能.Shen等[28 ] 利用静电纺丝制备了1D的石榴石纳米线,且制备了PEO基聚合物,在石榴石纳米线含量为5%时,室温电导率为5.53×10-5 S/cm,电化学窗口为4.75 V,在60 ℃下全电池循环以0.5 C倍率循环100圈后容量保持在123 mA· h/g.胡宁等[29 ] 以石墨烯为模板,利用液相法合成了石榴石纳米片并制备了PEO基聚合物,LLZO纳米片含量为15%且加入离子液体时,室温电导率为3.6×10-4 S/cm,且40 ℃下,全电池循环30圈后容量保持率为97.5%.南策文等[30 ] 利用静电纺丝制备了3D网络结构石榴石,以其为填料制备的PEO基聚合物电解质,室温电导率为1.8×10-4 S/cm,电化学窗口为4.5 V,利用该电解质组装的对称电池,电流密度为0.1 mA/cm2 ,室温下可以有效循环800 h.综上所述,纳米颗粒状、纳米纤维状石榴石型电解质被用来与PEO等聚合物电解质进行复合,从而降低PEO的结晶度,提高电解质的离子电导率,提升PEO基电解质的电化学性能.但是,具有特殊微观形态的石榴石型电解质与PEO的复合研究仍鲜有报道. ...
2
... 图1 为三维花瓣状石榴石型电解质的溶剂热法合成流程示意图,该方法分为两个主要过程,首先,通用溶剂热反应来合成粒径均匀的甘油酸盐球体La-Al-Zr-G.利用甘油与异丙醇溶剂热法制备甘油酸盐球体是一种比较普遍的方法.Saptiama等[31 ] 合成甘油酸锰、甘油酸锰-钴、甘油酸铜-钴、甘油酸铝等一系列甘油酸盐,反应温度均为180 ℃,时间为16 h.Ma等[32 ] 合成甘油酸铁微球的反应温度为190 ℃,反应时间为12 h.Septiani等[33 ] 合成甘油酸镍的反应温度和时间分别为180 ℃和16 h.大量的文献表明甘油酸盐球的反应温度为180~190 ℃,反应时间为12~16 h,基于此,本文中溶剂热的反应温度和时间分别为180 ℃和16 h.Al(NO3 )3 · 9H2 O、Zr(NO3 )4 · 3H2 O和La(NO3 )3 · 6H2 O作为金属离子源,按照化学计量比溶解于异丙醇与甘油的混合溶剂中,由于Zr(NO3 )4 · 3H2 O和La(NO3 )3 · 6H2 O在混合溶剂中的溶解度较低,为了得到澄清透明的溶液,因此先将这两种盐先后溶解于去离子水中,然后再加入异丙醇与甘油混合液中,搅拌均匀后将溶液转移到反应釜中.在溶剂热条件下,甘油分子在异丙醇中通过强分子间氢键自组装成球形准乳剂,从而促进纳米球的均匀生长[31 ] ,金属盐与甘油反应生成甘油酸盐,并以此为模板,得到球状的陶瓷粉体前驱体.第二个过程是立方石榴石相的形成过程,将过量LiOH· H2 O与甘油酸盐球体La-Al-Zr-G-1混合均匀,在高温800 ℃热处理,则得到三维花瓣状石榴石型电解质Li6.25 Al0.25 La3 Zr2 O12 . ...
... [31 ],金属盐与甘油反应生成甘油酸盐,并以此为模板,得到球状的陶瓷粉体前驱体.第二个过程是立方石榴石相的形成过程,将过量LiOH· H2 O与甘油酸盐球体La-Al-Zr-G-1混合均匀,在高温800 ℃热处理,则得到三维花瓣状石榴石型电解质Li6.25 Al0.25 La3 Zr2 O12 . ...
1
... 图1 为三维花瓣状石榴石型电解质的溶剂热法合成流程示意图,该方法分为两个主要过程,首先,通用溶剂热反应来合成粒径均匀的甘油酸盐球体La-Al-Zr-G.利用甘油与异丙醇溶剂热法制备甘油酸盐球体是一种比较普遍的方法.Saptiama等[31 ] 合成甘油酸锰、甘油酸锰-钴、甘油酸铜-钴、甘油酸铝等一系列甘油酸盐,反应温度均为180 ℃,时间为16 h.Ma等[32 ] 合成甘油酸铁微球的反应温度为190 ℃,反应时间为12 h.Septiani等[33 ] 合成甘油酸镍的反应温度和时间分别为180 ℃和16 h.大量的文献表明甘油酸盐球的反应温度为180~190 ℃,反应时间为12~16 h,基于此,本文中溶剂热的反应温度和时间分别为180 ℃和16 h.Al(NO3 )3 · 9H2 O、Zr(NO3 )4 · 3H2 O和La(NO3 )3 · 6H2 O作为金属离子源,按照化学计量比溶解于异丙醇与甘油的混合溶剂中,由于Zr(NO3 )4 · 3H2 O和La(NO3 )3 · 6H2 O在混合溶剂中的溶解度较低,为了得到澄清透明的溶液,因此先将这两种盐先后溶解于去离子水中,然后再加入异丙醇与甘油混合液中,搅拌均匀后将溶液转移到反应釜中.在溶剂热条件下,甘油分子在异丙醇中通过强分子间氢键自组装成球形准乳剂,从而促进纳米球的均匀生长[31 ] ,金属盐与甘油反应生成甘油酸盐,并以此为模板,得到球状的陶瓷粉体前驱体.第二个过程是立方石榴石相的形成过程,将过量LiOH· H2 O与甘油酸盐球体La-Al-Zr-G-1混合均匀,在高温800 ℃热处理,则得到三维花瓣状石榴石型电解质Li6.25 Al0.25 La3 Zr2 O12 . ...
1
... 图1 为三维花瓣状石榴石型电解质的溶剂热法合成流程示意图,该方法分为两个主要过程,首先,通用溶剂热反应来合成粒径均匀的甘油酸盐球体La-Al-Zr-G.利用甘油与异丙醇溶剂热法制备甘油酸盐球体是一种比较普遍的方法.Saptiama等[31 ] 合成甘油酸锰、甘油酸锰-钴、甘油酸铜-钴、甘油酸铝等一系列甘油酸盐,反应温度均为180 ℃,时间为16 h.Ma等[32 ] 合成甘油酸铁微球的反应温度为190 ℃,反应时间为12 h.Septiani等[33 ] 合成甘油酸镍的反应温度和时间分别为180 ℃和16 h.大量的文献表明甘油酸盐球的反应温度为180~190 ℃,反应时间为12~16 h,基于此,本文中溶剂热的反应温度和时间分别为180 ℃和16 h.Al(NO3 )3 · 9H2 O、Zr(NO3 )4 · 3H2 O和La(NO3 )3 · 6H2 O作为金属离子源,按照化学计量比溶解于异丙醇与甘油的混合溶剂中,由于Zr(NO3 )4 · 3H2 O和La(NO3 )3 · 6H2 O在混合溶剂中的溶解度较低,为了得到澄清透明的溶液,因此先将这两种盐先后溶解于去离子水中,然后再加入异丙醇与甘油混合液中,搅拌均匀后将溶液转移到反应釜中.在溶剂热条件下,甘油分子在异丙醇中通过强分子间氢键自组装成球形准乳剂,从而促进纳米球的均匀生长[31 ] ,金属盐与甘油反应生成甘油酸盐,并以此为模板,得到球状的陶瓷粉体前驱体.第二个过程是立方石榴石相的形成过程,将过量LiOH· H2 O与甘油酸盐球体La-Al-Zr-G-1混合均匀,在高温800 ℃热处理,则得到三维花瓣状石榴石型电解质Li6.25 Al0.25 La3 Zr2 O12 . ...
1
... LALZO陶瓷粉体的前驱体及粉体的形貌如图3 所示.图3 (a)~(b)是加入1 mL去离子水,溶剂热反应结束后,得到的镧-铝-锆甘油酸盐的SEM图,如图3 (a)所示为低分辨SEM图,图中镧-铝-锆甘油酸盐为球形,而且镧-铝-锆甘油酸球的尺寸较为均匀,且没有明显的团聚,分散性较好,如图3 (b)所示为高分辨SEM图,图中镧-铝-锆甘油酸球的粒径大约为800 nm,表面相对光滑.Lou等[34 ] 采用这种溶剂热方法合成活性电极材料,在溶剂热条件下,甘油分子在异丙醇中通过强分子间氢键自组装成球形准乳剂,从而促进纳米球的均匀生长.文献中报道的材料多为一种或两种的金属阳离子,合成具有三种金属阳离子的甘油酸球还较少有报道,多金属阳离子的甘油酸球合成难度增大,更为重要的是,本文中的Zr(NO3 )4 · 3H2 O和La(NO3 )3 · 6H2 O原材料难溶于异丙醇和甘油,必须先溶解于去离子水,经典溶剂热法所用的溶剂不含有任何去离子水,而水热法的溶剂则全部为去离子水,因此,严格说,本文应用的是溶剂热和水热的混合方法,因为去离子水的添加量相对于异丙醇和甘油较少,本文仍称之为溶剂热法,本文的溶剂热方法具有如下两个优点:第一,拓展了甘油酸球制备方法,制备了三金属元素的甘油酸球;第二,去离子水的引入,大大拓宽了原材料的选择. ...
1
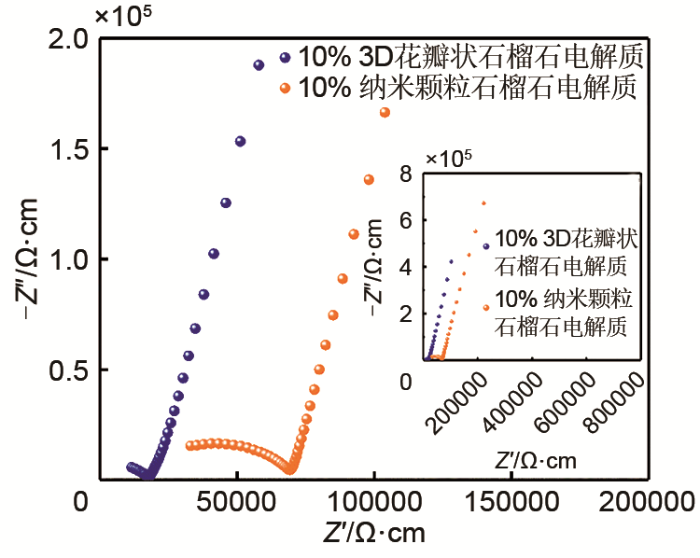
... 为了说明这种特殊微观形貌的石榴石型电解质的优越性,我们制备了两种复合固态电解质,即分别向PEO-LiTFSI聚合物中添加质量分数10%的三维花瓣状石榴石型电解质与纳米颗粒石榴石型电解质.图4 是两种复合固态电解质膜在25 ℃的电化学阻抗谱,测试条件为 10 mV的振幅,频率范围在1 MHz~1 Hz,如图4 所示,两个电化学阻抗谱都是由一个高频区半圆和一条低频区斜线组成,半圆代表本体电阻,斜线代表了双电层电容.通过计算,25 ℃下,含有10% 三维花瓣状石榴石型电解质的复合固态电解质的离子电导率为5.59×10-5 S/cm,约是添加相同含量颗粒状石榴石型电解质的复合固态电解质电导率的4倍(1.45×10-5 S/cm),这说明了这种三维花瓣状石榴石型电解质应用于复合电解质中的优越性.Guo等[35 ] 利用相场模拟、随机电阻网络模型以及Monte-Carlo模型等研究了石榴石/PEO复合电解质的渗流效应,说明了石榴石型电解质纳米颗粒与PEO聚合物基体之间的界面空间电荷区对离子电导率的影响,结果表明,孤立的陶瓷颗粒不会影响复合电解质的离子传输,只有形成连续的石榴石/PEO界面,才能形成连续的离子传输通道,从而大幅提升离子电导率,因此,必须有效提高陶瓷填料与聚合物基体的接触,才能实现优异的离子导电性能.本工作所制得的三维花瓣状石榴石型电解质作为填料时,由于纳米片随机在三维方向上组装在一起,可以最大限度的与PEO基体接触,产生三维的石榴石/PEO界面,形成三维的离子传输通道,大幅提升复合电解质的离子电导率. ...